
 |
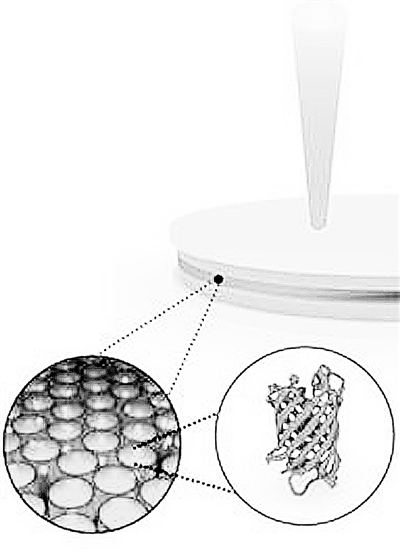
| 绿色荧光蛋白极化激元激光原理示意图:将活细胞产生的绿色荧光蛋白填充在微光腔中制成一层薄膜,光和电子能量混合产生准粒子。 |
科技日报北京8月22日电 (记者常丽君)一个由英德科学家组成的研究团队在最近出版的《科学·进展》杂志上发表论文称,他们首次将水母体内的荧光蛋白基因插入大肠杆菌基因组,利用转基因大肠杆菌产出了增强型绿色荧光蛋白(eGFP)并用来产生激光。研究人员指出,这一突破代表着极化激元激光领域的重大进步,其效率和光密度都比普通激光高得多,有望为研究量子物理学和光学计算开辟新途径。
据美国趣味科学网日前报道,传统的极化激元激光器用无机半导体做增益介质,必须致冷到极低温度;而有机发光二极管(OLED)显示器中的有机电子材料能在室温下工作,但需要有皮秒(万亿分之一秒)光脉冲来供能。研究团队开发的新激光器也能在室温下工作,但只需纳秒(10亿分之一秒)脉冲。
极化激元激光来自一种量子凝聚现象:激光增益介质中的原子或分子反复吸收发出光子,产生一种叫做极化激元的准粒子,在一定条件下变成一种联合量子态,从而发出激光。理论上极化激元激光需要的能量更少。
研究人员把转基因大肠杆菌产生的eGFP填充在许多光微腔里,作为一种“光泵”,能以纳秒速度发出闪光,使整个系统达到产生激光所需的能量。“光泵”能在达到激发阈值后,给设备注入更多能量以产生传统激光。该激光发明人之一、苏格兰圣安德鲁大学物理与天文学院教授马尔特·盖瑟说,皮秒脉冲的能量更合适,但制造起来要比纳秒脉冲难1000倍,他们的做法简化了很多制造工序。
盖瑟还指出,新方法的一个关键优点是,蛋白质分子的发光部分被一种纳米大小的圆柱形外壳保护着,让它们彼此间不会互相干扰,分子结构很适合在高亮度下工作,更容易发出激光。但目前的激发阈值还太高,今后经过改进,最终可让极化激元激光器的激发阈值比传统激光器低得多,这样效率会更高,发光更致密。


 下一版
下一版




